Introduction
L’encéphalopathie aiguë (EA) est un processus pathobiologique responsable d’un dysfonctionnement global – et souvent réversible – de l’encéphale, d’installation rapide (< 4 semaines).1 Elle peut être la conséquence de multiples étiologies, incluant des causes métaboliques, toxiques et infectieuses. Cliniquement, l’EA se manifeste par un large spectre pouvant aller de l’état confusionnel au coma. Il s’agit d’une urgence diagnostique car le pronostic peut être fatal. L’EA est l’une des complications neurologiques les plus fréquentes du Covid-19 chez les patients hospitalisés.2 Face à ces constatations, la controverse sur l’origine de l’EA associée au Covid-19 s’est rapidement ouverte. Nous discutons dans cet article les différentes hypothèses étiologiques de l’EA associée au Covid-19, incluant les comorbidités préexistantes ou les complications liées à l’hospitalisation, et finalement un lien direct ou indirect avec l’infection par le virus SARS-CoV-2 (figure 1).
Encéphalopathie postvirale: un retour sur les grandes pandémies
L’association entre infection et encéphalopathie est connue depuis l’antiquité: Hippocrate déjà (460-377 av. J.-C.), dans le livre IV de son Prognostikon, avait remarqué que le delirium (φρενιτις, « phrénite ») pouvait accompagner la fièvre.3 Les mécanismes reliant infection et l’EA peuvent être directs, par invasion par des pathogènes neurotropes (par exemple, le virus Herpès simplex), ou indirects, quand un microorganisme non neurotrope déclenche une réaction inflammatoire ou dysimmunitaire, aboutissant in fine à l’EA.4
Des EA ont été rapportées au cours d’infections par des virus respiratoires comme le virus de la grippe H1N1, et le coronavirus SARS-CoV. Celles-ci ont été décrites à la phase aiguë de la maladie, et sont alors le reflet d’un effet cytopathique direct du virus, ou alors sont apparues plus tardivement dans l’évolution, évoquant un mécanisme dysimmun.5 Le virus SARS-CoV a un potentiel neurotrope direct, caractéristique partagée par d’autres coronavirus humains (HCoV) (par exemple, le HCoV-229E et le HCoV-OC43). Il est possible que le SARS-CoV-2, taxonomiquement très similaire au SARS-CoV, soit aussi neuro-invasif.6 La pandémie d’encéphalite léthargique (maladie de Von Economo), qui a sévi de 1917 à 1927, quasi simultanément à celle de la « grippe espagnole » (1918-1920), a récemment fait l’objet d’un regain d’intérêt.7 Le virus potentiellement responsable de cette encéphalite épidémique n’est toujours pas identifié, et l’association étiologique avec la grippe A (H1N1) reste débattue. Les manifestations aiguës de l’encéphalite léthargique comprenaient des symptômes neurologiques focaux et neuropsychiatriques (par exemple, une EA) telles qu’on peut les voir dans le Covid-19. De plus, un nombre important de patients présentaient un syndrome parkinsonien des années plus tard, comme l’a décrit Oliver Sacks (1933-2015).8 La possibilité des séquelles neurologiques à distance de l’infection aiguë de SARS-CoV-2 mérite donc de ne pas être sous-estimée.7
Encéphalopathie aiguë et covid-19: un épiphénomène ?
En mars 2020, une équipe française décrivait chez 58 patients admis aux soins intensifs (SI) pour un syndrome de détresse respiratoire aiguë (SDRA, ou ARDS pour Acute Respiratory Distress Syndrome) associé au Covid-19, une prévalence de 14 % d’états confusionnels à l’admission, et 67 % après la levée de la sédation.9 Cette proportion dépasse le tiers d’états confusionnels post-SI rapportés dans des études précédentes avant la pandémie SARS-CoV-2.10 Les comorbidités et les complications peuvent agir comme facteurs précipitants (tableau 1). Nous évoquons ici les principales situations pouvant favoriser le développement d’une EA dans le Covid-19.
Insuffisance rénale
Plus de 20 % des patients hospitalisés pour un Covid-19, et plus de 50 % de ceux qui nécessitent une prise en charge aux SI développent une insuffisance rénale aiguë.11 L’origine est probablement multifactorielle, soit par action directe sur le rein (par exemple, néphrotoxicité du virus ou de certains médicaments, comme le lopinavir/ritonavir), ou indirecte (par exemple, hypovolémie, surcharge volémique). L’accumulation de toxines urémiques, de cytokines pro-inflammatoires, les troubles électrolytiques et le cumul de médicaments peuvent amener à une augmentation de la perméabilité de la barrière hémato-encéphalique (BHE) avec infiltration de molécules neurotoxiques.12
Hyponatrémie
L’hyponatrémie, fréquemment sur le syndrome de sécrétion inappropriée d’hormone antidiurétique (SIADH)13, est une étiologie classique d’EA, et survient chez presque un quart des patients avec pneumonie à SARS-CoV-2.14
Hypoxémie
Le Covid-19 est, in primis, une maladie respiratoire. L’hypoxémie est fréquente et grave comme le souligne l’étude européenne « COVID-ICU » dans laquelle plus de 50 % des patients aux SI pour ventilation mécanique présentent un SDRA modéré.15 L’hypoxémie est reconnue comme facteur de risque de déficit neuropsychologique.16
Complications thrombotiques
Chez les patients avec un Covid-19, les événements thromboemboliques cérébraux (dont l’incidence, selon la plus grande étude à ce jour, est de l’ordre de 16 %) pourraient également participer à la pathogenèse de l’EA.17 Ces complications pourraient être la conséquence d’une endothélite.18
Médicaments
Certains médicaments peuvent induire une EA.19 La mise en place de nouveaux protocoles thérapeutiques, afin de pallier la pénurie de certains médicaments (par exemple, le propofol) nous a poussés à utiliser davantage de benzodiazépines (par exemple, le midazolam) notamment délirogènes.20 Cela pourrait avoir joué un rôle non négligeable dans le développement d’EA lors de la première vague. De plus, l’utilisation fréquente de la dexaméthasone peut favoriser les troubles neuropsychiatriques.
Présentations cliniques de l’encéphalopathie aiguë associée au covid-19
Deux principaux profils cliniques se distinguent selon la sévérité de la présentation.
Retards de réveil aux soins intensifs
Cette présentation concerne typiquement les patients ayant eu un SDRA sévère, dans les jours suivant la levée de la sédation, se traduisant par un coma sans explication métabolique, hypoxémique ou médicamenteuse.21 L’évolution clinique de ces patients est très variable et les facteurs de vulnérabilité n’ont été que partiellement identifiés. Si certains évoluent de manière défavorable avec un décès, d’autres vont vers un tableau de mutisme akinétique, alors que certains présentent une évolution spontanément favorable avec une sortie du coma. Il faut néanmoins être particulièrement vigilant devant les pièges de ces présentations cliniques, et ne pas confondre un tableau d’akinétisme global dans le cadre de l’état confusionnel aigu avec un état végétatif ou encore un mutisme akinétique avec une aphasie.
États confusionnels dans les unités conventionnelles et les soins intermédiaires
Une certaine proportion de patients présente un état confusionnel (hypo-/hyperactif) pouvant précéder l’atteinte pulmonaire. De notre expérience, les patients hospitalisés en raison d’un syndrome confusionnel présentent un plus fort risque d’évolution défavorable sur le plan respiratoire et systémique, suggérant qu’il puisse s’agir d’un facteur de mauvais pronostic. Par ailleurs, il n’est pas rare de retrouver des signes neurologiques focaux transitoires, pas forcément associés à des AVC.22
Examens complémentaires et pathologie
À ce jour, les examens paracliniques n’ont pas retrouvé de « signature » spécifique permettant d’identifier les patients présentant une EA associée au Covid-19. Certains profils semblent cependant se détacher.
Imagerie cérébrale par résonance magnétique
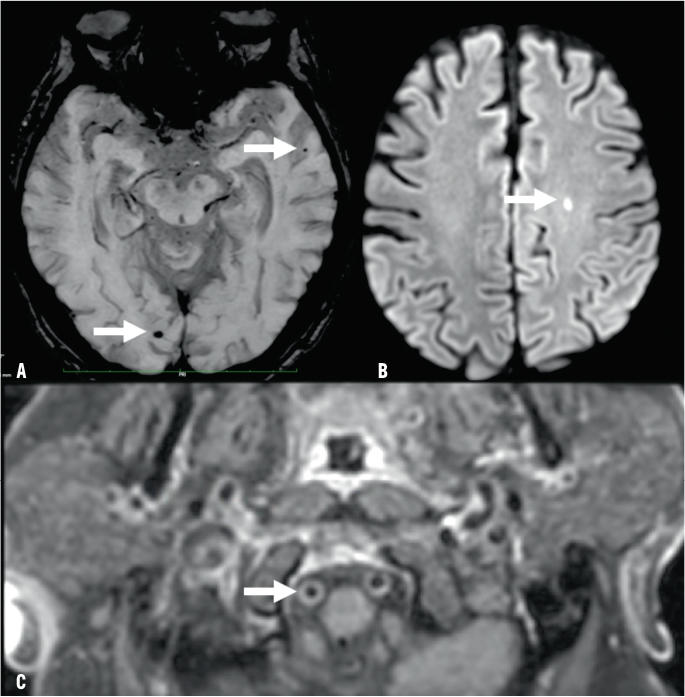
Les anomalies les plus fréquemment retrouvées sont des lésions ischémiques ou des microsaignements.23 Des prises de contrastes vasculaires, de signification encore incertaine, ont été décrites chez les patients avec EA. Ces rehaussements ont une morphologie caractéristique avec une atteinte circonférentielle et régulière des vaisseaux sans lésion ischémique parenchymateuse en aval de la prise de contraste, suggérant une atteinte de l’endothélium vasculaire de type endothélite. Il s’agit donc d’une atteinte différente des vasculites cérébrales classiques, notamment par l’absence de caractère sténosant ou « en collier de perles » typique. Cette observation, décrite pour la première fois à Genève,21 s’est confirmée par la suite dans une cohorte strasbourgeoise.24 Il est néanmoins important de relever que le lien exact entre ces prises de contrastes vasculaires suggestives d’endothélite cérébrale et la présentation clinique de cette EA reste incertain (figure 2).
Analyse du liquide céphalo-rachidien
Une altération de la BHE est observée chez la majorité des patients encéphalopathes, démontrée par l’augmentation du quotient albumine (tableau 2)25 ainsi que celle de certaines cytokines pro-inflammatoires.26 La cellularité du LCR est normale dans la grande majorité des cas, et la détection du virus SARS-CoV-2 par Reverse Transcriptase PCR (RT-PCR) est typiquement absente, bien que déjà rapportée de manière anecdotique.27 La présence d’une synthèse intrathécale d’immunoglobulines spécifiques anti-SARS-CoV-2 est en général absente, sauf exception. L’analyse détaillée du LCR ne permet pas actuellement de confirmer l’hypothèse selon laquelle l’EA associée au Covid-19 serait en lien direct avec une infection méningo-cérébrale par le SARS-CoV-2.
Électroencéphalogramme
Bien que les crises d’épilepsie représentent une complication exceptionnelle chez les patients avec un Covid-19,28 les EEG réalisés dans le cadre d’encéphalopathie peuvent retrouver un ralentissement global, thêta ou delta aspécifique.29
Encéphalopathie et Covid-19: « évidences » neuropathologiques ?
Les trouvailles neuropathologiques les plus fréquemment observées sont une gliose réactive, une infiltration lymphocytaire périvasculaire, des lésions hypoxiques et ischémiques, ainsi que des infarctus corticaux microscopiques.30 L’endothélite intracérébrale n’a, pour l’instant, été décrite que dans un nombre limité de cas.18 Les manifestations neuropathologiques peuvent résulter de l’effet cytopathogène du SARS-CoV-2, ou de la réponse inflammatoire induite par l’infection virale.30 La présence du virus au niveau cérébral (recherche de protéines ou de matériel génétique) a été suggérée dans une minorité d’études.31 Une « contamination cérébrale passive » liée à l’infection virale systémique ne peut pas être exclue. Le commentaire d’une équipe genevoise et internationale de neuropathologues montre bien l’absence d’unanimité quant à l’interprétation des données neuropathologiques dans le Covid-19.32
Hypothèses physiopathologiques (figure 3)
Inflammation et dysfonctionnement endothélial
Un dysfonctionnement de l’endothélium vasculaire, via un mécanisme inflammatoire ou viral direct, responsable d’une rupture de la BHE, est une hypothèse physiopathologique actuellement très explorée.33 La présence d’une vulnérabilité endothéliale préexistante pourrait par ailleurs favoriser l’apparition de ce tableau clinique. L’endothélium vasculaire est sensible à l’inflammation et aux dérivés réactifs de l’oxygène (Reactive Oxygen Species, ou ROS). La dysfonction endothéliale – dont la première étape est l’activation endothéliale qui se caractérise par un phénotype anormal pro-inflammatoire et prothrombotique des cellules endothéliales – est volontiers favorisée par certaines comorbidités comme les maladies métaboliques, le syndrome d’apnées du sommeil ou l’athérosclérose.34 Chez les patients avec Covid-19 sévère, l’endothélium vasculaire pourrait être lésé par le biais de cytokines mais également par le virus lui-même. Ceci entraînerait une rupture de la BHE et un passage de cytokines dont certaines ont un potentiel neurotoxique.35 Cette hypothèse est concordante avec les observations paracliniques et pathologiques décrites plus haut: la prise de contraste vasculaire sur l’IRM cérébrale, l’augmentation du quotient albumine et des cytokines dans le LCR, la réponse favorable dans certains cas aux traitements anti-inflammatoires stéroïdiens21 et les résultats de la neuropathologie mettant en évidence une dysfonction endothéliale.24
Atteinte immune médiée
Une autre hypothèse intéressante est celle d’une atteinte dysimmunitaire. La chronologie des symptômes (qui apparaissent parfois tardivement par rapport à l’infection) et, dans certains cas, la réponse aux traitements immunomodulateurs plaident en faveur d’un mécanisme dysimmunitaire. Par ailleurs, des cas de maladies autoimmunes (comme l’encéphalomyélite aiguë disséminée et des polyradiculonévrites aiguës démyélinisantes) ont été décrits suite à une infection au SARS-CoV-2.36
Atteinte directe par le virus
Bien que moins probable, l’hypothèse d’une atteinte directe par le virus a été soulevée. Des mécanismes d’entrée par voie transnasale via les nerfs olfactifs (transport trans-synaptique dans le lobe frontal), ou par voie hématogène via la rupture de la BHE, ont été suggérés.6
Traitements
Au-delà des mesures habituelles de prise en charge de l’état confusionnel, aucun traitement étiologique n’a été validé dans l’EA associée au Covid-19. Cependant, suite à des observations encourageantes, il a été proposé, à Genève notamment, un traitement expérimental de corticostéroïdes à haute dose chez des patients sélectionnés selon un algorithme décisionnel après concertations multidisciplinaires.
Conclusion
L’EA associée au Covid-19 est une complication neurologique fréquente, retrouvée chez les patients avec Covid-19 sévère, soulevant la question de son origine. Si l’hypothèse physiopathologique prépondérante est celle d’un dysfonctionnement cérébral d’origine inflammatoire, impliquant un orage cytokinique systémique, la question de la spécificité de l’infection à SARS-CoV-2 est encore source de débat, notamment celui d’un lien avec une endothélite cérébrale. Il ne fait aucun doute que les comorbidités, les médicaments et les complications métaboliques sont des facteurs aggravants. Chez des patients soigneusement sélectionnés, l’utilisation de stéroïdes à haute dose semble avoir un effet favorable durant la phase aiguë. Enfin, les séquelles neurologiques et neuropsychologiques à moyen et long termes sont encore inconnues incluant possiblement dans la controverse un lien entre confusion, inflammation et pathologies neurodégénératives.37
Conflit d’intérêts:
Les auteurs n’ont déclaré aucun conflit d’intérêts en relation avec cet article.
Implications pratiques
• L’encéphalopathie aiguë associée au Covid-19 est une complication neurologique fréquente, particulièrement chez les patients âgés, hospitalisés
• Il est important de rechercher activement les différentes causes d’encéphalopathie et de les prendre en charge rapidement
• L’hypothèse physiopathologique de l’encéphalopathie aiguë associée au Covid-19 implique des mécanismes inflammatoires affectant l’intégrité de la barrière hémato-encéphalique
• L’utilisation de corticostéroïdes à haute dose pourrait être un traitement de l’encéphalopathie aiguë associée au Covid-19, bien que son efficacité ne soit pas encore démontrée