Introduction
L’année 2020 a vu la propagation exponentielle et pandémique de SARS-CoV-2, responsable du Covid-19. Un des goulots d’étranglement a été l’accès aux tests diagnostiques, limité pour des raisons diverses, comme un déficit en ressources humaines ou des tests eux-mêmes. On estime que lors de la première vague, moins d’un·e Romand·e infecté·e sur dix a pu être diagnostiqué·e (étude Serocovid1), bloquant de facto toute velléité de traçage des contacts, pourtant pierre angulaire d’une bonne gestion épidémique.2
Les tests rapides antigéniques offrent une accessibilité diagnostique facilitée (coût, manipulation) dans les structures de soins périphériques et dans la communauté, permettant un rendu du résultat en 15-20 minutes. Ils nécessitent un frottis nasopharyngé fait par une personne formée pour cela ou un frottis nasal antérieur qui peut être fait par la personne elle-même (qui doit cependant bien suivre la procédure).
Bien que la sensibilité de la PCR soit globalement plus élevée que celle des tests rapides antigéniques, la méthode comporte plusieurs inconvénients. La technique est chère (depuis le début de l’épidémie, elle aurait déjà coûté environ un demi-milliard de francs à la Confédération), nécessite un plateau technique et humain de haut niveau, retarde le rendu des résultats de plusieurs heures à plusieurs jours et ne tient pas compte de la persistance de l’ARN viral plusieurs semaines à plusieurs mois après l’infection, ce qui peut mener à un résultat positif sans rapport avec la clinique ou le risque de transmission. Quel que soit le type de test, une méthode buccale ou salivaire permettrait un prélèvement nettement plus confortable que le frottis nasopharyngé.
Afin d’explorer la performance diagnostique des tests rapides antigéniques, ainsi que la dynamique de cette performance en fonction du niveau potentiel de contagiosité des patients, de la durée des symptômes et du type de prélèvement, une étude comparative prospective, RaDiCo, a été menée au cours du dernier trimestre 2020 à Unisanté et Vidy-Med à Lausanne.3 Cet article met en perspective ses résultats et en discute les implications pratiques pour la clinique et le dépistage. Des données d’une expérience pilote avec des tests antigéniques rapides sur des échantillons nasaux, oropharyngés et bucco-salivaires sont aussi présentées.
Description, méthodes et résultats
L’étude RaDiCo avait pour but de comparer les performances diagnostiques de 3 tests antigéniques rapides nasopharyngés (TDR NP) (Standard-Q de Biosensor/Roche, Panbio de Abbott et COVID-VIRO de AAZ-LMB) et la PCR buccosalivaire (BS) avec la PCR nasopharyngée (NP). Ont été recrutés des patient·e·s de plus de 18 ans suspects de Covid-19 consultant en filière ambulatoire selon les critères d’inclusion de coronacheck.ch, la plateforme évaluant la nécessité pour une personne de se faire tester sur les cantons de Vaud, Valais et Neuchâtel. Chaque patient·e inclus a bénéficié d’un TDR-NP réalisé sur place par le soignant et de deux PCR analysées au laboratoire de microbiologie du CHUV. Les différentes marques de TDR-NP ont fait l’objet d’une rotation régulière jusqu’à atteindre les 100 positifs chacune, afin de remplir les standards OMS4 et suisses de validation de TDR.5 La procédure d’autoprélèvement buccosalivaire supervisé a été établie après analyse de la littérature et calibrage au cours d’une phase pilote. Les sensibilités des TDR-NP et des PCR ont été évaluées, d’une part, contre PCR-NP (test de référence utilisé dans la plupart des études) et, d’autre part, contre une mesure de référence composite comprenant tout test positif. Les résultats ont ensuite été stratifiés par catégorie de charge virale (CV) et durée des symptômes. Le calcul de la CV est effectué à partir du Cycle threshold (Ct); 104, 105 et 106 copies/ml correspondent respectivement à des Ct de 33, 30 et 26.6
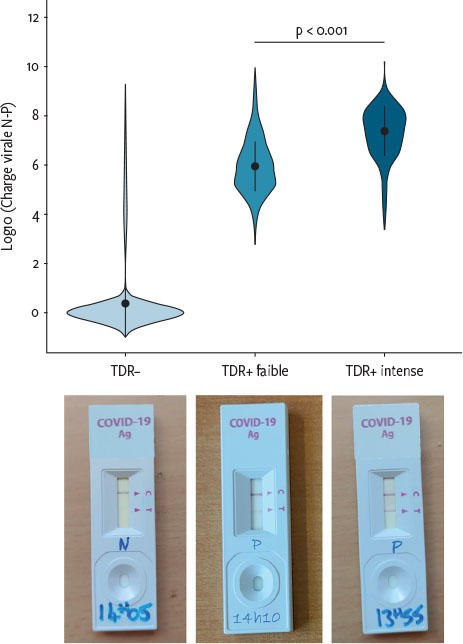
928 patient·e·s ont été inclus dans l’étude. 385 (41,5 %) sont revenus positifs par au moins un test, 327 (35,2 %) par TDR, 369 (39,8 %) par PCR BS et 372 (40,1 %) par PCR NP. Avec un seuil de CV ≥ 106 cp/ml, les taux de détection étaient respectivement de 31,6, 30,3, 31,4 et 31,5 %, sans différence statistiquement significative. La sensibilité globale pour les TDR-NP comparés à la PCR-NP était de 87,4 % et de 96,5 % (93,6-98,3 %) pour les individus considérés comme clairement contagieux (≥ 106 cp/ml) (voir figure 1 montrant la sensibilité en fonction de la charge virale). Parmi les marques, le STANDARD-Q a montré 92,9 % de sensibilité par rapport à la PCR-NP, le Panbio 86,1 % et le COVID-VIRO 84,1 %, ou 96,6, 97,8 et 95,3 % avec le seuil de CV de 106 cp/ml. L’intensité de la bande du test rapide était en lien avec la CV, la médiane de cette dernière étant de 3 × 107 cp/ml si l’intensité était forte et de 7 × 105 cp/ml si elle était faible (figure 1). Aucun·e patient·e avec des traces de virus (CV < 104 cp/ml) n’a été détecté·e par les tests rapides. La spécificité face à la mesure composite était de 100 % (IC 95 %: 99,3-100 %), deux TDR avec la PCR-NP correspondante négative ayant eu leur résultat positif confirmé par PCR-BS.
Les sensibilités des PCR-BS et NP étaient respectivement de 95,8 et 96,6 % comparées à la mesure composite. Une large majorité des patient·e·s a consulté durant la première semaine de symptômes (moyenne de 2,6 jours du premier symptôme). La sensibilité des TDR diminuait légèrement avec l’augmentation de la durée des symptômes (et donc la baisse de la charge virale), variant entre 90 et 80 %, donc au-dessus du seuil recommandé par l’OMS et l’OFSP (Office fédéral de la santé publique).
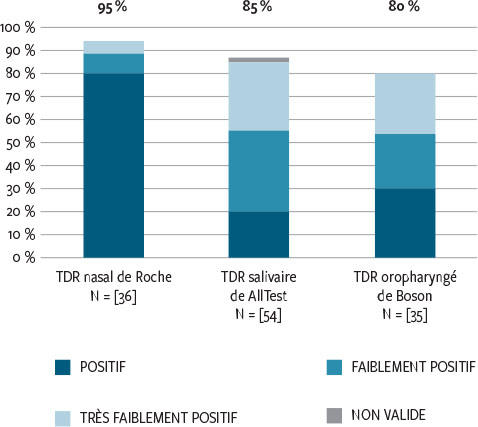
En ce qui concerne les nouveaux tests antigéniques rapides nasaux, salivaires et oropharyngés, essayés chacun sur quelques dizaines de personnes en comparant le résultat à celui du meilleur des TDR nasopharyngés (celui de Biosensor/Roche), ils ont montré une sensibilité de 94,4 % pour le test Standard-Q nasal, 85,2 % pour le test rapide salivaire de Hangzhou AllTest Biotech et 80 % pour le test rapide oropharyngé de Xiamen Boson Biotech (figure 2).
Discussion
En ce qui concerne les patient·e·s avec une charge virale considérée comme significative d’un point de vue clinique et épidémiologique, la sensibilité des TDR-NP s’est avérée excellente (> 95 %). Si l’on inclut également les patient·e·s avec une charge virale basse, qui ont un risque très faible d’être contagieux, la sensibilité restait très bonne (> 85 %), supérieure aux seuils de validation requis par l’OMS et l’OFSP.4,5 Ces résultats variaient légèrement d’une marque de test à l’autre malgré une distribution des charges virales similaire parmi les personnes testées, le test de Biosensor distribué par Roche étant le plus performant avec une sensibilité de 93 %. À noter que, les TDR détectant la partie moins variable de la protéine N (la nucléocapside), leur performance n’est pas affectée par les variants qui circulent actuellement et qui se distinguent, eux, par des mutations affectant principalement la protéine S.
La spécificité dans notre étude s’est révélée parfaite, ce qui n’exclut pas la possibilité qu’un faux positif puisse se produire de temps en temps. Le fait que les patients TDR+/PCR-NP– étaient positifs par PCR salivaire suggère cependant que la probabilité qu’une personne TDR+/PCR– soit en fait un vrai positif (la PCR faussement négative étant le plus souvent due à un frottis nasopharyngé sous-optimal) est plus élevée que celle qu’elle soit un faux positif. De plus, du fait qu’elle alourdit encore le travail sur le terrain, la recommandation actuelle de l’OFSP de confirmer les TDR+ chez une personne asymptomatique par une PCR pose donc le risque qu’une personne avec une charge virale significative ne soit alors pas mise en isolement.
Une controverse existe quant au seuil à partir duquel une personne devrait être considérée comme non contagieuse, plusieurs auteurs faisant le lien entre la cultivabilité et l’infectiosité.7-11 Il pourrait en ressortir une recommandation à considérer comme « négative » une personne asymptomatique positive avec une CV < 105 cp/ml (ou un Ct ≥ 30) hors quarantaine postcontact, une personne étant non ou très peu contagieuse si le Ct est au-dessus de 24 à 26.8,1°,11 En dehors des patient·e·s hospitalisé·e·s et/ou immunodéficient·e·s, il y a donc un avantage à utiliser les TDR qui évitent de détecter les personnes ayant une PCR positive persistante pendant des semaines, voire des mois, alors qu’elles sont en phase postinfectieuse et non contagieuses depuis longtemps.12 Cela permettrait à ces personnes de pouvoir à nouveau accéder aux services indispensables qui exigent un test négatif, qu’ils soient médicaux (opération élective, réhabilitation…) ou transfrontaliers (voyage à l’étranger pour des motifs impératifs, par exemple familiaux).
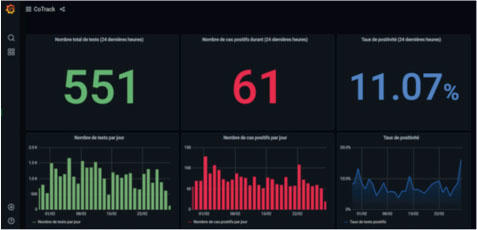
Quel que soit le seuil choisi pour considérer un test PCR négatif, la sensibilité imparfaite des TDR au stade aigu est largement compensée par la possibilité d’un usage à grande échelle (que ce soit pour le diagnostic dans les pharmacies, écoles, prisons, institutions communautaires et auprès des personnes sans domicile fixe, ou le dépistage de masse dans la communauté). De plus, l’obtention et la transmission d’un résultat en 2-3 minutes pour la plupart des TDR positifs et en 15 minutes pour s’assurer que le test est vraiment négatif permettent une stratégie de dépistage interventionnelle plutôt que de surveillance passive, la décision d’isoler une personne et de tester ses contacts sur place et/ou de les mettre en quarantaine pouvant se prendre immédiatement. Dans le canton de Vaud, ceci permet également un suivi en temps réel de ces tests via la plateforme informatique (monitoring.unisante.ch, figure 3) – plateforme qui a ensuite donné naissance à un outil similaire permettant le suivi en temps réel de la vaccination sur le canton de Vaud (vaccination.datacovidvaud.ch)).
La PCR buccosalivaire a révélé une performance qualitative comparable à la PCR nasopharyngée, la charge virale mesurée sur un même patient étant cependant inférieure d’environ 1 log et demi. La réplication virale ayant lieu dans l’épithélium respiratoire, il est donc attendu d’en trouver moins dans des sites distants (bouche). Notre étude confirme ainsi la performance similaire de la PCR-BS comparée à la NP dans la première semaine de l’infection trouvée dans d’autres études,13 la sensibilité de la PCR-BS diminuant ensuite avec la charge virale, au décours de l’infection aiguë, ce qui a l’avantage d’éviter de détecter inutilement un certain nombre de patients non contagieux.14
Les résultats de RaDiCo et des études similaires ont amené à modifier la stratégie de testing du canton de Vaud. Les filières diagnostiques sont passées avec succès à l’usage majoritaire des TDR (essentiellement Biosensor/Roche), alors que la PCR ambulatoire n’est nécessaire en vue d’un génotypage que dans certains cas précis, tels que la suspicion d’un échec vaccinal (test positif chez une personne symptomatique ≥ 7 jours après la 2e dose) ou d’une réinfection (test positif chez une personne symptomatique ≥ 3 mois après un Covid documenté).
La bonne performance du TDR de Biosensor/Roche avec frottis prolongé des deux narines (perte de sensibilité d’environ 5 % par rapport au TDR nasopharyngé de Biosensor/Roche) va permettre un accès facilité au dépistage dans la phase épidémiologique que nous traversons actuellement, avec maintenant une stabilisation des indicateurs et un accès élargi aux vaccins. Le nouveau TDR salivaire All Test®, qui est déjà utilisé en Allemagne et a montré une sensibilité de 85 % par rapport au TDR de Biosensor/Roche dans notre évaluation informelle à Unisanté, est actuellement en cours de validation par l’OFSP.
Conclusion
Lors d’une suspicion de Covid chez un·e patient·e non sévère, ne nécessitant donc pas de prise en charge particulière du point de vue clinique, le but est avant tout de savoir s’il·elle est contagieux·se pour l’isoler le plus rapidement possible et mettre en quarantaine ses contacts. Une sensibilité moindre sur les faibles CV des TDR-NP relève plus de l’avantage que de l’inconvénient pour éviter de diagnostiquer des personnes non contagieuses dans la phase postinfectieuse. L’étude RaDiCo, ainsi que la littérature actuelle, fournissent un bon niveau de preuve que les tests TDR nasopharyngés sont une alternative fiable et moins chère, à privilégier sur les PCR (nasopharyngées ou salivaires) pour le diagnostic du Covid-19 dans la pratique ambulatoire et communautaire.
Conflit d’intérêts:
Les auteurs n’ont déclaré aucun conflit d’intérêts en relation avec cet article.
Implications pratiques
• Les tests antigéniques rapides (TDR) pour le SARS-CoV-2 détectent plus de 95 % des personnes contagieuses dans un délai de 15 minutes, ce qui permet de décider d’un isolement immédiat et de quarantaine des contacts en cas de positivité. Cette méthode peut donc être privilégiée en milieu ambulatoire et communautaire
• Chez des patients symptomatiques, la PCR buccosalivaire a une sensibilité qualitative équivalente à la PCR nasopharyngée pour détecter une infection à SARS-CoV-2. Elle peut donc être utilisée sans restriction
• Chez les personnes asymptomatiques hors quarantaine de contact, une PCR positive est souvent le reflet de la phase post-infectieuse, ces personnes n’étant alors plus contagieuses, parfois depuis longtemps